高校化学 化学結合
イオン結合
[編集]
塩化ナトリウムNaClでは、ナトリウム原子は電子の1個を出して陽イオンのナトリウムイオンNa+になっている。塩素原子Clは、ナトリウムから放出された電子を受取り、陰イオンの塩化物イオンCl-になっている。
この と との電気的な引力(クーロン力)によって、分子が互いに引き付け合いとが交互に配置することによって の結晶が作られている。
このように、陰イオンと陽イオンによる電気的な引力による結合をイオン結合といい、そのイオン結合をしている陰イオンと陽イオンからなる結晶をイオン結晶(ionic crystal)という。イオン結晶では、陽イオン(positive ion)と陰イオン(negative ion)が規則的に配列をしている。
性質
[編集]イオン結合は非金属元素と金属元素の化合物で発生しやすい。元素の電気陰性度の差が1.8以上の場合はイオン結合になると考えていい。
イオン結晶の性質
[編集]イオン結合の電気的な引力は強いためイオン結晶の融点は高い。イオン結晶は電気を通さないが、イオン結晶を加熱して溶融したものや、イオン結晶を水に溶かした水溶液は電気を通しやすい。これは、自由に動けるようになったイオンが電気を通すためである。
組成式
[編集]イオン結晶は分子では無いため分子式を持たないが、イオン結晶を構成する原子数の比を使った組成式で表すことが出来る。イオン結晶の組成式では左側に陽イオン、右側に陰イオンを書く。
例えば、塩化ナトリウムは、ナトリウムイオンと塩化物イオンが1:1の割合で構成されているため、その組成式は である。
一般に、陽イオン と陰イオン のイオン結晶の組成式は となる。なぜなら、イオン結晶は全体で電気的に中性であるため、陽イオンの価数 × 陽イオンの個数 = 陰イオンの価数 × 陰イオンの個数 が成り立つためである。
イオン結晶の名称は、陰イオン、陽イオンの順に、そのイオンの名前をつなげることで命名する。ただし、「-(物)イオン」の部分は省略する。
例えば、 は塩化物イオンとナトリウムイオンの組み合わせなので、名前は塩化ナトリウムである。
は硫酸イオンとナトリウムイオンの組み合わせなので、名前は硫酸ナトリウムとなる。
共有結合
[編集]共有結合は、おおむね、以下のような仕組みである。 例として、水素分子での水素原子どうしの結合で説明する。
- 水素原子が近づく。
- それぞれの原子核は、相手原子の価電子(valence electron)を引き合う。
- 価電子は、もとの原子を引き付けるから、結局、電子を仲立ちとして、原子核どうしが近づく。原子核どうしが近づいた結果、電子軌道の一部は共有されるので、電子殻の一部が共有される。
- 共有された電子殻の一部では、水素原子の合計2個の価電子は1対になっている。このように価電子が対になったものを電子対(でんしつい,electron pair)という。
ここで注意すべきなのは、電子どうしには引力が生じない、ということである。原子核どうしにも引力は生じない。あくまでも電荷の異なる粒子どうしの、原子核と電子とが電気引力を及ぼしているのである。同種の電荷である原子核どうしには反発力が生じている。同様に、同種の電荷である電子どうしにも反発力が生じている。
このように価電子を仲立ちとして、電子を共有することによって生じる結合を共有結合(covalent bond)という。
対電子は、なにも結合だけではなく、1個の原子の電子殻上でも、価電子が多い場合は、対電子が生じる。 たとえば、L殻の原子では、5個の価電子を持つN原子は1組の電子対をもつ。6個の価電子を持つO原子は2組の電子対をもつ。7個の価電子を持つF原子は3組の電子対をもつ。比較のため、同じL殻のC原子を例に出すと、4個の価電子を持つC原子は0組の電子対をもつ。
非共有電子対
[編集]
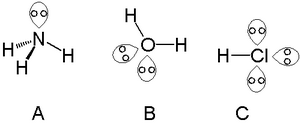
電子対は、必ずしも全てが結合に寄与するわけではない。結合に寄与する電子は、他の原子の価電子と対を作る場合のみである。したがって、同じ原子内の電子どうしで対を作っている場合は結合に寄与しない。このような同じ原子内の価電子どうしで対を作っている電子対を非共有電子対(ひきょうゆうでんしつい,shared electron pair)という。
不対電子
[編集]対を作らない価電子を不対電子(unpaired electron)という。 たとえばL殻の原子では、4個の価電子を持つ炭素原子Cは不対電子を4個もつ。5個の価電子を持つ窒素原子Nは不対電子を3個もつ。6個の価電子を持つ酸素原子Oは不対電子を2個もつ。7個の価電子を持つフッ素原子Fは不対電子を1個もつ。 なお、K殻原子である水素原子の不対電子は1個である。
共有結合を行う電子は、不対電子である。たとえば4個の不対電子をもつ炭素原子Cは、水素Hと結合してメタン CH4 を作る事ができる。
3個の不対電子を持つ窒素原子Nは、水素原子Hと結合すれば、アンモニアNH33 を作ることができる。
また、水素との結合のように、各原子が1個ずつ相手原子に不対電子を提供して共有電子対になった結合を単結合(たんけつごう)という。
構造式では単結合を1本の棒線で表す。たとえば水素分子は
- HーH
である。棒線の1本あたり、1組の共有電子対を表している。 なお、このような共有電子対を表す線を価標(かひょう,bond)という。
多重結合
[編集]二重結合
[編集]
ニ酸化炭素CO2 でのCとOと結合を考える。不対原子は、O原子には2個あり、C原子には4個ある。 そうすると、1個のC原子と1個のO原子との結合に参加する不対原子は、O原子からは2個であり、C原子からはOの不対電子の相手をするC原子の不対電子が2個ほど必要である。
そうすると、結合は4個の不対電子から2対の共有電子対が形成される。このように2対の共有電子対が形成される結合を二重結合(double bond)という。
構造式で表す場合、二重結合は = のような、上下の長さが等しい2本線で表す。(つまり2本の価標である。)棒線の1本あたり1組の共有電子対を表している。
ニ酸化炭素CO2の構造式は
- O=C=O
である。 なお、構造式は、分子の実際の形には対応しない。あくまで構造式は共有電子対の共有の様子を表示したものである。
三重結合
[編集]
たとえば窒素分子N2のN原子どうしは3組の共有電子対で結合している。3組の共有電子対による結合を三重結合(triple bond)という。構造式では、3本の価標で表す。
配位結合
[編集]
アンモニアNH3を水や濃塩酸HClと反応させるとアンモニウムイオンNH4+が生じる。 これはアンモニアの非共有電子対に、水素イオンが吸引された結果である。水素イオンは価電子を放出して正電荷になっているので、電子に引きつけられる。 このように非共有電子対に、価電子が空のイオンが吸引されてできる結合を配位結合(はいい けつごう ,coordinate bond)という。
NH4+の結合について、アンモニウムイオンNH4+の持つ結合N-Hの4個の結合は、4個とも同等であり、配位結合したあとは区別できない。 このような理由から、配位結合は共有結合の一種と見なされる。
- オキソニウムイオン
水H2Oや、希塩酸などの酸性溶液では、少しだけイオン化をしていて、H3O+とOH-とにイオン化をしている。このH3O+は、H2OにHが配意した配位結合である。このH3O+をオキソニウムイオン(oxonium ion)という。
極性
[編集]
水素分子H2や塩素分子Cl2のように同種の原子の共有結合で出来た結合において、電子対はどちらにも片寄らず、したがって電荷はかたよらない。 このような電荷の片寄りのない分子を無極性分子(むきょくせいぶんし,nonpolar molecule)という。
いっぽう、塩化水素分子HClでは、塩素に電子は片寄っている。その結果、H原子は、すこしばかりの正の電荷 δ+ を持ち、塩素原子は少しばかりの負の電荷 δ- を持つ。このように分子内に電荷の片寄りのある状態を極性(きょくせい,polarity)と言い、極性の有る分子を極性分子(polar molecule)という。
- 三原子以上の場合の極性
ニ酸化炭素CO2ではC=Oの結合には極性があるが、分子全体ではO=C=Oが直線上の形状のため、2個のC=O結合の極性同士が反対向きになり、極性が打ち消し合う。したがって、分子全体ではニ酸化炭素は極性をもたない無極性分子である。このように原子数が3子以上の場合は、分子の形状が極性に関係してくる。
水H2Oは極性分子である。分子全体では折れ線の形になっている。
メタンCH4は無極性分子であり、正四面体の構造をとる。正四面体の4個の頂点に対応する位置に水素原子Hがあり、正四面体の中心に対応する位置に炭素Cがある。
水素結合
[編集]
16族原子のOと結合したH2Oは、同じ16族原子との化合物のH2SやH2Seとくらべて、沸点が特に高い。 17族のFとの化合物のHFは同じ17族原子の HCl などとくらべて沸点が特に高い。 15族のNとの化合物のNH3も同様に、他の同属化合物より沸点が特に高い。 このような現象の仕組みを述べる。
O、F、Nとも電気陰性度の高い元素である。 例としてHFを解説する。フッ化水素HFはフッ素の電気陰性度が大きく、電子はフッ素に吸引される。この結果、水素原子は静電荷にかたよる。この大きく分極した水素を仲立ちとして、周囲のHF原子のFを吸引することで、物質全体として強い結合をする。 これを水素結合(hydrogen bond)という。水素結合は、相手の原子がO、F、Nなどの電気陰性度の高い場合である。 電気陰性度が3番目に高いClは、原子半径が大きいため、電荷密度が小さい。そのため、水素結合は起こらない。

金属
[編集]金属では、電子は金属全体を動ける。電子殻の視点で見れば、実際に電子殻を周辺の多くの原子と共有している。共有結合と違って特定の原子間で電子を共有しているのでは無い。金属原子は、電子の広がらせやすさが大きい。 金属内の電子は、その結晶全体を動け、特定の原子には拘束されない。このような電子を自由電子(free electron)という。 また、自由電子による金属同士の結合を金属結合(metallic bond)という。
金属の性質
[編集]金属の特徴的な性質は、展性と延性や金属光沢、また、熱や電気を伝えやすいといったようなものがある。
展性と延性
[編集]金属を強く叩く加工をすると、箔状に広げることが可能だが、箔状に広げても、金属がつながったままで、割れたり切れたりしにくく、叩いても金属がつながったままで広げやすい性質を展性(てんせい,ductility)という。また、金属を伸ばして線状に引き伸ばしても、切れにくくつながったままの性質を延性(えんせい,malleability)という。 この展性や延性は、自由電子による。金属結合が自由電子による結合なので、加工によって変形をしても、原子の配列が変わっただけで、金属全体では自由電子を共有しつづけるので、金属結合を維持し続けるからである。
金属光沢
[編集]金属には光沢が有る。これは、金属表面で光の反射が起こるからである。より正確に言うと、光をいったん吸収して、その直後に再放出をするので、反射をする。金属によっては、全ての波長を反射せずに波長の一部の光を吸収するので、その結果、金属は色みを帯びて見えることになる。
銀では、ほぼすべての入射光を反射するので、銀白色に見える。(白色とは、可視光の波長が全て揃っている光の状態である。) 銅や金など、色づいて見える金属は、入射光の一部の波長の光を金属が吸収している事による。
その他の性質
[編集]金属は自由電子の働きで熱や電気をよく伝えるため導体である。さらに、単体のケイ素Siや、ゲルマニウムGeのように、導体と絶縁体の中間的な性質をもつものを半導体という。
金属は一般に温度が高くなればなるほど電気抵抗が大きくなる。これは、金属原子の熱運動が激しくなり、自由電子の移動を妨げるためである。また、金属の中には、低温状態で電気抵抗が0になるものがあり、この現象を超伝導という。









